Hairiness control
Insects are less likely to take a bite out of a hairy plant. Not only did the leaves of plants with lots of hairs, also called trichomes, change in an obstacle course. But this obstacle course is also littered with chemical mines. Those spread a sticky and deadly substance when triggered. Not something an insect wants to deal with, exactly as the plant likes it.
This makes growing hairy crops for breeders and farmers interesting. As there would be less need to intervene against insect pest. Unfortunately, lots of crops have lost their hairy appearance over time. As such researchers are busy with finding out how plants get more trichomes.
In a new study named ‘The SlGRAS9-SlMYC1 regulatory module controls glandular trichome formation and modulates resilience to pest in tomato’, French and Chinese researchers study which genes exactly determine the number of hairs loaded with such a chemical mine.
With GRAS9 less hairs
The first thing the researchers did was analysing which gene regulators were active in the trichomes of tomato plants. One was sticking out: GRAS9. To be sure that GRAS9 indeed regulates the number of trichomes, the researchers analysed the amount of GRAS9 in 4 plants with lots of trichomes and in 4 plants with hardly any trichomes. Especially in plants with hardly any trichomes had lots of GRAS9.
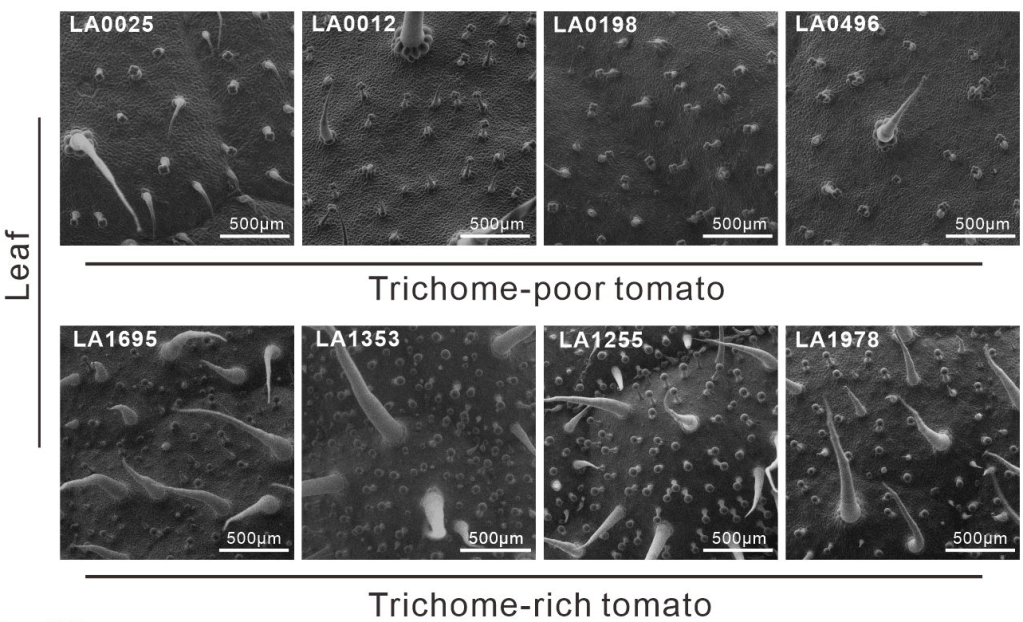
This suggests that GRAS9 prevent the development of trichomes. To confirm this the researchers created plants without GRAS9. Those plants were very hairy. In addition, they also produced more lading for the chemical mines. But GRAS9 did not appear to regulate those genes directly.
To find the middlemen, or in this case gen regulator, the researchers dived in the literature. It was found that in an earlier study that one of the genes that GRAS9 regulates in MYC1.
MYC1 for hairiness
To confirm that MYC1 is indeed the link that the researchers are looking for, the researchers checked that MYC1 is active in the trichomes. What indeed turned out to be the case. Subsequently the researchers created plants without or with more MYC1. Plants with more MYC1 were hairy just like the GRAS9 missing plants. But when MYC1 was absent, then there were hardly any trichomes. The researchers also crossed the plants missing GRAS9 with those missing MYC1. The prodigy of those plants looked like MYC1 missing plants. Confirming that MYC1 was indeed the link the researchers were looking for.
The big question was if more trichomes also resulted in less insect pests. To analyse this the researchers exposed the plants to aphids and spider mites. Plants without GRAS9 or with more MYC1 were less damaged by aphids and spider mites. This in contrast to plants without MYC1 who were more damaged.
GRAS9 controls thus together with MYC1 the number of trichomes on a plant. This makes them interesting targets for breeders. Because hairy plants are more resistant against insect pests.
Literature
Shi, Y., Wang, Y., Pan, Y., Deng, C., Zeng, T., Su, D., Lu, W., Lin, Y., Han, J., Deng, W., Wu, S., Liu, Y., Li, N., Li, J., Dong, B., Abid, G., Bouzayen, M., Pirrello, J., Li, Z. and Huang, B. (2025), The SlGRAS9-SlMYC1 regulatory module controls glandular trichome formation and modulates resilience to pest in tomato. Plant J, 122: e70183. https://doi.org/10.1111/tpj.70183


